Utføre virksomheten i samsvar med gjeldende lovgivning og selskapsreguleringer
I Bayer er vi dedikerte til integritet i alle våre forretningsmessige disposisjoner. Integritet er et kjerneelement i våre verdier og i vår kultur. Vi overholder all gjeldende lovgivning og reguleringer og etterlever de høyeste standarder for etisk atferd.
Våre prinsipper for bedriftsatferd
-
Vi konkurrerer rettferdig i alle markeder
-
Vi opptrer med integritet i alle våre forretningsdisposisjoner
-
Vi balanserer økonomisk vekst med økologisk og sosialt ansvar
-
Vi overholder handelsreguleringer som regulerer vår globale virksomhet
-
Vi sikrer like muligheter innen verdipapiromsetning
-
Vi sikrer korrekt regnskapsføring og dokumentasjon
-
Vi behandler hverandre rettferdig og med respekt
-
Vi beskytter og respektere immaterielle rettigheter
-
Vi handler i Bayers interesse
-
Vi beskytter og sikrer personopplysninger
Ytelser til helsepersonell
|
|
Felles forskning tjener pasienter og samfunnetSamarbeid mellom legemiddelindustrien og helsepersonell har ført til tallrike innovative legemidler og endret forutsetningene for at ulike sykdommer kan påvirke våre liv. Vi i Bayer er overbevist om at nært samarbeid med og kontinuerlig utdanning av helsepersonell er en nøkkel til å oppnå ytterligere resultater for pasientene som vi bestreber oss på å hjelpe. |
Legemiddelindustrien – Helsepersonell: Et sterkt regulert forholdNår vi samarbeider med medisinske eksperter, overholder vi gjeldende lover og regler som klart redegjør for interaksjon mellom industrien og helsepersonell, for eksempel lover for helsesektoren og bransjekodeks. Disse reglene er dessuten tillagt visse åpenhetsregler, så som Sunshine Act i USA, EFPIA Disclosure Code i EU og forskjellige lokale rapporteringsforpliktelser. Vi respekterer fullt ut helsepersonells integritet og uavhengighet. |
|
|
|
Implementering av EFPIA Disclosure CodeSom medlem av den europeiske sammenslutningen av legemiddelindustri og foreninger (EFPIA) og i overenstemmelse med vår virksomhets verdigrunnlag, støtter vi EFPIA Disclosure Code fullt ut. I henhold til denne kodeks vil Bayer offentliggjøre betalinger og ytelser til helsepersonell og organisasjoner på Bayers lokale hjemmesider |
|
|
Hvordan Bayer samarbeider med helsepersonell
Legemiddelindustrien og personell i helsesektoren samarbeider i en rekke aktiviteter innenfor preklinisk forskning, klinisk utvikling, klinisk praksis og vurdering av behandlingsresultater.
Gjennom sin nære kontakt med pasientene besitter helsepersonell uvurderlig ekspertkunnskap om behandlingsresultater og sykdomsbekjempelse. Dermed spiller de en avgjørende rolle i vår innsats for å forbedre sykdomsforløp, behandlingsmuligheter og –resultater for pasientene.
Samarbeid – eksempel 1: Kliniske studier
Pasienter behøver riktige legemidler
Pasienter kan kun dra virkelig nytte av den enorme mengden uvurderlige medisinsk kunnskap som eksisterer, når våre interne eksperter arbeider tett sammen med eksterne forskere og helsepersonell. Vi er overbevist om at felles bruk av ekspertise vil hjelpe oss til å få en bedre forståelse av de viktigste sykdommene og utvikle bedre legemidler raskere. Den behandlende lege og annet helsepersonell gjennomfører kliniske forsøk på studiesentre I henhold til reglene for kliniske studier, som er godkjent av helsemyndighetene, legefaglige organisasjoner og etiske komiteer. De er dermed den viktigste lenken til de deltagende pasientene og er ansvarlige for innsamling av data. Den ekspertise og tid som stilles til rådighet av helsepersonell og helseorganisasjoner gjennom en klinisk studie, skal kompenseres på riktig måte.
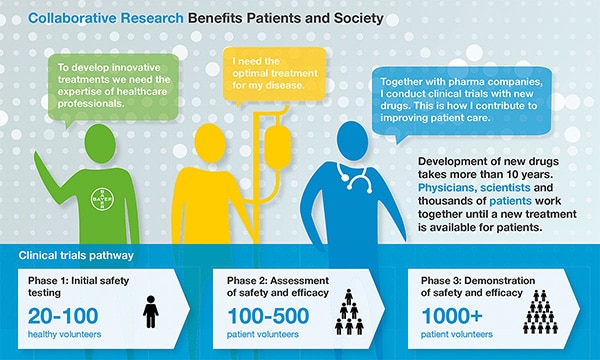
Les mer om kliniske studier her
Samarbeid – eksempel 2: Støtte til videreutdanning av leger
Pasienter behøver de best opplyste legene
Bayer utvikler innovative legemidler. Nye behandlingsformer er komplekse og skal introduseres og forklares til helsepersonell for å sikre ansvarlig bruk. Derfor støtter vi videreutdannelse av helsepersonell på kongresser og seminarer. Det bidrar til at leger har adgang til den nyeste medisinske forskningen og dermed er i stand til å gi pasienten de aller beste behandlingsmulighetene. Først da kan vi oppfylle vår forpliktelse til å sikre riktig bruk av våre nye behandlinger. Vitenskapelige events er et av mange bidrag til legers utdannelse.
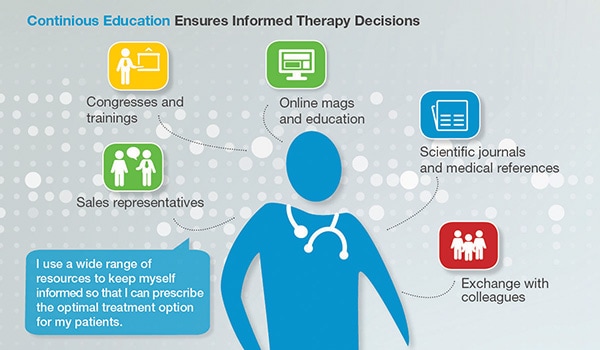
Hva EFPIA Disclosure Code handler om
Bayer støtter større åpenhet i forholdet mellom legemiddelindustrien og helsesektoren og garanterer derfor overholdelse av EFPIA Disclosure Code.
|
|
40 ledende europeiske virksomheter i 33 land har forpliktet seg til EFPIA Disclosure CodeEFPIA Disclosure Code (fullt navn: EFPIA Disclosure Code of Transfers of Value from Pharmaceutical Companies to Healthcare Professionals and Healthcare Organizations) er en frivillig forpliktelse hvor alle EFPIA’s medlemsbedrifter, herunder Bayer, offentliggjør alle direkte og indirekte, monetære og ikke-monetære, ytelser som foretas i forbindelse med utvikling og markedsføring av reseptbelagte medisiner til mennesker. |
|
|
KompensasjonsstørrelseLeger og helsepersonell blir kompensert for sin ekspertise og de ytelser de leverer til legemiddelindustrien. Størrelsen på betalinger og ytelser avhenger av aktivitetens art, det faglige nivå og forbrukt tid. De tillatte beløpsstørrelser er avhengig av ulike faktorer, som lokalt inntektsnivå, lovgivning og gjeldende kodeks. Det bærende prinsippet er at vederlag for mottatte tjenester skjer etter en rettferdig markedsverdi for å sikre at honorarer ikke misbrukes til å få urimelig innflytelse på helsepersonell i deres behandlingsbeslutninger. |
|
|
Individuell eller samlet offentliggjøring?Ytelser til leger og helsepersonell rapporteres på individuell eller samlet basis. I samsvar med norske bransjeregler offentligjøres verdioverføringer individuelt for det enkelte helsepersonell med grunnlag i selskapenes berettigede interesse i slik offentliggjøring, se LMIs bransjeregler kapittel 26. Ytelser innenfor området «Forskning og utvikling» blir alltid rapportert på et samlet nivå, som beskrevet i EFPIA Disclosure Code. |
|
|
PersonvernBayer respekterer personvern og beskyttelse av personopplysninger fullt ut. Derfor sørger vi for at de innsamlede personopplysninger beskyttes i henhold til personvernlovgivningen og kan kontrolleres av lokale og globale myndigheter. Omfattende sikkerhetsforanstaltninger sørger for at personopplysninger er beskyttet mot eksternt misbruk og manipulasjon. Videre er tilgang til personopplysninger beregnet for offentliggjøring, begrenset til medarbeidere som er ansvarlige for datainnsamling og rapportering. |
|
|
Fullstendig offentliggjøringVi er av den overbevisning at kun en fullstendig offentliggjøring gir et riktig bilde av vårt forhold til en lege eller annen person i helsesektoren. Derfor vil vi ikke offentliggjøre delvise data på individuell basis. Enhver uenighet om offentliggjøring av en spesifikk aktivitet behandles av Bayer som generell uenighet om offentliggjøring. I stedet vil alle ytelser innberettes på et samlet grunnlag i henhold til EFPIA’s rapporteringsforskrifter. |
Verdioverføringer til helsepersonell
I samsvar med EFPIA Disclosure Code vil Bayer rapportere åpent om de verdioverføringer som er gjort til helsepersonell og helseorganisasjoner knyttet til utvikling og kommersialisering av reseptbelagte legemidler.
De rapporterte data gjelder verdioverføringer i fire kategorier:
| Kategorier | Verdioverføringer | |
| Helsepersonell (HCP) | Helseorganisasjoner (HCO) | |
| Donasjoner | - | Monetære eller ikke monetære |
| Arrangement |
|
|
| Tjenester og konsultasjoner |
| |
| Forskning og utvikling | Avgifter eller utlegg for kostnader som er knyttet til oppdraget eller konsultasjonen, feks reise og losji | |
Tilgang til data for Norge
| 2021 | 2022 | 2023 |
| PDF download | PDF download | PDF download |
EFPIA Disclosure Code gjelder alle medlemsselskaper og innebærer at selskapene vil rapportere de verdioverføringer som er gjort til helsepersonell og helseorganisasjoner i et forhåndsbestemt format. Likevel kan rapporteringsmetodene variere mellom selskapene på grunn av selskapenes ulike interne prosesser. Denne metodebeskrivelsen forklarer hvordan Bayer i Norge har tilrettelagt informasjonen.
1. Bakgrunn
Metodebeskrivelsen er strukturert og delt inn i ulike kapitler, avhengig av området og spørsmål hvor vi forklarer med eksempler som tydelig illustrerer metoden vi har brukt. Ved eventuelle uklarheter om overføring av en verdi skal offentliggjøres eller ikke, har vi full åpenhet som målsetting. Bare om verdioverføringen åpenbart ikke faller inn under regelverket, vil den ikke bli publisert i rapporten.
2. Rettslig grunnlag for behandling og offentliggjøring av verdioverføring på individuelt grunnlag
I samsvar med LMIs bransjeregler skal verdioverføringer til helsepersonell offentliggjøres individuelt. Det rettslige grunnlaget for behandling og offentliggjøring av personopplysninger knyttet til verdioverføringer er den berettigede interesse selskapet har i offentliggjøringen. Medlemsfirma har en berettiget interesse i offentliggjøring av verdiverføringene som medfører at behandlingen av personopplysningene, herunder offentliggjøring av verdioverføringene til helsepersonell, er nødvendig. Se i den forbindelse bla. de hensyn som ligger bak EFPIAs regelverk og krav om offentliggjøring, og Stortingets behandling av sak om dette i 2019. Samtidig veier ikke helsepersonells eventuelle interesser i hemmelighold eller deres grunnleggende rettigheter/friheter tyngre enn de berettigede interessene bak offentligjøring, se personopplysningsloven § 1 og GDPR artikkel 6 nr.1 bokstav f).
Helsepersonell informeres om offentliggjøringen før eller i forbindele med at avtale om verdioverføringer inngås. Forøvrig kommer personopplysningslovens regler til anvendelse. Dersom det er helt spesielle forhold knyttet til det enkelte helsepersonell, kan det gi grunnlag for å protestere mot offentligjøringen (se vilkår som følger av GDPR artikkel 21). Dersom slike omstendigheter foreligger, skal verdioverføringen rapporteres aggregert.
Helseorganisasjon som er enkeltpersonsforetak behandles i denne sammenheng som individuelt helsepersonell.
3. Rapporteringen - hva er inkludert?
3.1 Reseptbelagte legemidler
Direkte og indirekte overføring av verdi til HCP og HCO som kommer fra aktiviteter med Bayer. Det er foreløpig kun aktiviteter som er knyttet til reseptbelagte legemidler til mennesker som inkluderes.
3.2 Hva er en verdioverføring?
En verdioverføring blir definert som både en pengeoverføring og en ikke-pengeoverføring gjort på grunnlag av avtale mellom HCP / HCO og Bayer. Dette kan være lønn, honorar eller annen godtgjørelse for utført arbeid, samt kompensasjon for utgifter i forbindelse med gjennomføring av oppdrag (f.eks. reise og opphold), donasjoner samt sponsing av helsearrangementer.
3.3 Hva rapporteres under HCP?
Overføringer i form av lønnsutbetalinger til HCP samt utgifter i forbindelse med utførelsen av et oppdrag vil bli rapportert på den enkelte HCP.
Offentliggjøringen vil inneholde følgende informasjon: Fullt navn, adresse på hovedpraksis/arbeidssted, samlet verdi på overføringer og en detaljert oversikt over overføringene inndelt i ulike kategorier; honorar for oppdrag og konsulenttjenester, bidrag til kostnader ved arrangementer, herunder registreringsavgifter, samt reise- og overnattingskostnader.
3.4 Hva rapporteres under HCO?
Honorar og tilknyttede utgifter som faktureres fra enkeltpersonforetak, foreninger, aksjeselskaper, kommandittselskaper samt øvrige selskapsformer vil offentliggjøres under HCO. For oppdrag utført i tjenesten rapporteres beløp som er betalt til organisasjonen eller avdelingen under HCO. Donasjoner og sponsing til helsevesenet rapportens også under HCO.
Rapporten vil inneholde:
- Fullstendig navn
- For helseorganisasjon: registreringssted (Brønnøysundregistrene)
- Land der virksomheten finner sted
- Fysisk adresse til virksomheten
3.5 Hva er inkludert i lønn/ honorarer?
Lønn og honorar rapportert i samsvar med det som er avtalt i en skriftlig kontrakt. Lønn vises som brutto godtgjørelse for oppdraget, inkludert sosiale avgifter.
3.6 Hva inngår i «tilknyttede utgifter»?
Kostnader i forbindelse med et konsulentoppdrag f.eks. reise og opphold som HCP/HCO har i forbindelse med oppdraget. Dersom HCP eller HCO har hatt en utgift i form av en registreringsavgift i forbindelse med oppdraget, vil dette også rapporteres under ”utlegg til kostnader forbundet med oppdraget eller konsultasjonen, f.eks. reise og losji”. Måltider inngår ikke.
3.7 Når rapporteres verdioverføringer?
Rapportering av verdioverføring fra foregående kalenderår skjer senest 6 måneder etter utgangen av det aktuelle år, f.eks. publiseres alle verdioverføringer som skjedde i 2023 (januar-desember) ved utgangen av juni 2024. Verdioverføringen bokføres etter kontantprinsippet dvs. når pengene er utbetalt og ikke når hendelsen fant sted. I unntakstilfeller kan rapportering skje ett år senere (f.eks ved korrigeringer)
3.8 Hvor lenge er rapporten offentlig tilgjengelig?
Rapporten vil være tilgjengelig i tre år etter publiseringen. Rapporten kan endre seg etter publiseringen om nødvendig for å korrigere eventuelle feil.
3.9 Overføringer av verdi over landegrenser.
All overføring av verdi som skjer over landegrenser, rapporteres på samme måte som lokale verdioverføringer. HCP / HCOs hovedarbeidsplass eller kontorplass er avgjørende for hvilket land overføring av verdi skal rapporteres i. F.eks. hvis Bayer AG i Tyskland ansetter en norsk HCP / HCO for et konsulentoppdrag vil verdioverføringer fra oppdraget rapporteres på HCP / HCO i Norge og i den norske rapportmalen. Denne tilnærmingen gjelder også hvis en Bayerenhet utenfor Europa engasjerer en norsk HCP / HCO.
3.10 Valuta
Rapporteringen gjøres i norske kroner, NOK. I de tilfeller hvor overføring av verdi er skjedd i en annen valuta, rapporteres verdioverføring i norske kroner til en gjennomsnittskurs den måneden da utbetalingen ble gjort. Verdioverføringen skjer i henhold kontantprinsippet - se pkt 4 nedenfor.
3.11 Skatt og arbeidsgiveravgift
Verdioverføringer vil bli rapportert eksklusive merverdiavgift. Inntektsskatt og trygdeavgift vil bli inkludert i det rapporterte beløp.
4. Rapporteringsperioden
4.1 Kontantprinsippet
Data rapporteres generelt etter kontantprinsippet, det vil si at de rapporteres i det året verdioverføringene faktisk fant sted. Verdioverføringene vil bli rapportert basert på datoen de blir utbetalt. Dette kan være når en inngående faktura betales eller når betaling skjer via lønn. I tilfeller hvor faktura kommer tidlig i begynnelsen av påfølgende år, tilstreber vi å inkludere verdioverføringene så langt det er mulig i rapporteringen knyttet til det siste året, i stedet for å rapportere dem som verdioverføringer som kan henføres til inneværende år. I unntakstilfeller kan rapportering også skje senere (f.eks. i forbindelse med rettelser).
Kontantprinsippet bestemmer også hvem som ansees som mottakerne av verdioverføringen. F.eks. hvis onkologisk avdeling ved Oslo universitetssykehus har mottatt en verdioverføring for en sponsing eller donasjon, og det er Oslo
universitetssykehus sin økonomiavdeling som sender faktura til Bayer, vil verdien av overføring blir rapportert på Oslo universitetssykehus som en juridisk enhet, og ikke på onkologisk avdeling.
5. Sponsing
5.1 Hva rapporteres under sponsing?
Verdioverføringer til HCO for sponsing av spesifikke arrangementer i regi av tredjeparter der Bayer får en motytelse. Det kan f.eks. være en stand i et utstillingsområde. Det som rapporteres er summen som er avtalt i skriftlig avtale mellom HCO og Bayer.
5.2 Tredjepartsarrangør
Når en tredjepart organiserer administrasjon og fakturering av sponsormidler, vil dette være en direkte overføring av verdi til en administrerende tredjepart og samtidig en indirekte overføring av verdi til den HCO som drar nytte av verdioverføringen. Dette er rapportert under "sponsing" av den aktuelle HCO.
5.3 Sponsing av flere HCO
I de tilfeller vi sponser flere HCO’er vil beløpet deles opp og rapporteres likt fordelt mellom HCO’ene, om ikke annet framgår tydelig av avtale.
6. Forskning og utvikling
6.1 Hva er inkludert i forskning og utvikling?
Verdioverføringer relatert til planlegging eller gjennomføring av ikke-kliniske studier, kliniske studier (fase I-V) eller ikke-intervensjonsstudier som omfatter innsamling av pasientdata fra helsevesenet eller for deres regning, inkluderes i denne rapporteringspost.
6.2 Hvordan vil forskning og utvikling rapporteres?
Forskning og utvikling vil bli rapportert som en totalsum i kategorien ”FoU” uten noen spesielle opplysninger om mottakeren av verdioverføringen.
6.3 Hvordan offentliggjøres verdioverføringer når vi bruker CRO (Clinical Research Organisation)?
Ved bruk av et eksternt klinisk forskningsfirma, et CRO, som genererer indirekte overføring av verdi til HCP / HCO fra Bayer, vil dette bli rapportert under aktuell HCP / HCO, på samme måte som beskrevet ovenfor.
7. Markedsundersøkelser
Markedsundersøkelser er alltid gjort anonymt og vil ikke bli rapportert.
8. Donasjoner
Bayers interne regler for donasjoner er restriktive, derfor er sannsynligheten liten for at det forekommer donasjoner. Hvis dette allikevel skjer, rapporteres de i kategorien "Gaver og donasjoner til helseorganisasjoner". Stipend som gis til HCO vil også bli rapportert under kategorien "Gaver og donasjoner til helseorganisasjoner".
Bayer collaborations with patient organizations in Norge during the year 2023